1. Conceitos básicos e introdutório para o ensino de química
-
1AQUÍMICA
Texto em PortuguêsQUÍMICA
Química é a ciência que estuda a composição, estrutura, propriedades da matéria, as mudanças sofridas por ela durante as reações químicas e a sua relação com a energia. Tudo o que existe no universo é formado por química.
Pode parecer que a Química limita-se à teoria e às pesquisas de laboratório ou à produção industrial. Mas ela é uma das ciências que está mais presente em nosso cotidiano e dentro de nós mesmos. No nosso organismo, também ocorrem diversas transformações químicas. A Química é útil em inúmeras atividades, como, por exemplo, na agricultura, onde os agricultores a utilizam para melhorar a acidez do solo. Os médicos também precisam do conhecimento químico para reconhecer a composição das substâncias utilizadas como medicamento.
Só para citar alguns exemplos, a Química contribui para o desenvolvimento e produção de medicamentos que salvam vidas, de produtos de higiene e limpeza, de combustíveis que levam ao desenvolvimento de nossa sociedade e de meios de produção mais eficazes. Além disso, ela está presente na composição dos alimentos que consumimos (sejam naturais ou artificiais) e nas reações do nosso organismo, como a digestão.
A Química é uma ciência de três níveis fundamentais:
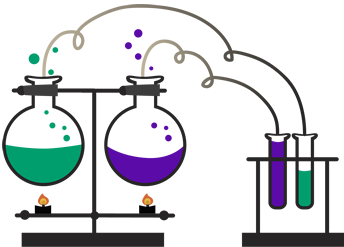
- I. Macroscópico: Transformações que podemos observar as mudanças sem o uso de equipamentos, com por exemplo uma fruta que apodrece, um remédio que mudou de cor pois já passou da validade, a lataria de um carro que está enferrujada pois sofreu ação do meio ambiente.
- II. Microscópico: Transformações que não podem se observadas sem o uso de equipamentos específicos. Neste nível os cientistas tentam interpretam o que não podemos ver, para explicar as transformações macroscópicas e tentar controlá-las. Importante perceber então, que as transformações que acontecem no nível microscópico são responsáveis pelas transformações no nível macroscópico.
- III. Simbólico: A Química parece que tem uma língua própria. Nesta ciência usam-se símbolos próprios, tais como fórmulas moleculares e equações para representar as transformações estudadas.

-
1BÁTOMO
Texto em PortuguêsÁTOMO
A palavra átomo, tem sua origem no grego e significa indivisível. Os filósofos da grécia antiga, propunham que todas as coisas são formadas por partículas muito pequenas e indivisíveis.
Hoje, podemos dizer que o átomo é a menor parte que constitui a matéria. Toda matéria então, é formada por minúsculas partículas, os átomos. Ou seja, Tudo é formado por átomo. Exemplos: o sal, o açúcar, as plantas, o ar, tudo, tudo é formado por átomos, inclusive nós!
Existe um número finito de átomos na natureza, aproximadamente 120 tipos de átomos.
A combinação entre átomos iguais ou diferentes origina os materiais. Importante: os átomos são formados por partículas fundamentais: prótons neutrons e elétrons.
Precisamos ter em mente que esses são apenas modelos que servem para entendermos a estrutura do átomo, suas propriedades e características. Mas não podemos afirmar que o modelo seja exatamente a imagem do átomo.
X
 Fonte: https://gifimage.net/atomo-gif-animado-8
Fonte: https://gifimage.net/atomo-gif-animado-8
-
Texto em Português
1CMOLÉCULA
MOLÉCULA
Na natureza os átomos se combinam para ficarem estáveis. Essa combinação entre átomos iguais ou diferentes são as moléculas. Então podemos dizer que a molécula é um grupo de átomos.
Alguns exemplos de moléculas é quando dois átomos de oxigênio se combinam para formar uma molécula de oxigênio e quando um átomo de carbono combina com dois átomos de oxigênio para formar uma molécula de dióxido de carbono.
Os químicos representam as moléculas por fórmulas químicas, exemplo: H2O (água) , NaCl (sal de cozinha), C2H6O (álcool comum).
X

-
Texto em Português
1D SUBSTÂNCIA
SUBSTÂNCIA
Todo material é formado por grupos de átomos, que são as moléculas. Podemos ter materiais formados por moléculas iguais e outros materiais formados por dois, três, vários tipos de moléculas.
Quando a matéria é formada somente por moléculas iguais temos uma substância. A substância então é um grupo de moléculas iguais.
Quando a matéria é formada por duas, três, vários tipos de moléculas, ou seja moléculas diferentes temos uma mistura.
A substância é um pedaço de matéria formado por moléculas iguais, e por isso apresenta propriedades e características bem definidas, que a torna única, diferente de qualquer outra substância, como por exemplo a temperatura que derrete e como a temperatura que ferve.
X
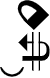
-
1ESUBSTÂNCIA SIMPLES
Texto em PortuguêsSUBSTÂNCIA SIMPLES
Na natureza os átomos se combinam e formam as moléculas. Quando átomo iguais se combinam formam-se moléculas que representam substâncias simples. Exemplo, o planeta Terra é protegido dos raios solares por uma camada de gás que conhecemos como camada de ozônio. Você sabia que o ozônio é formado por três átomos do Oxigênio? Por isso o ozônio é uma substância simples, pois é formado por átomo do mesmo tipo, iguais. Oxigênio + Oxigênio + Oxigênio = O3 = gás ozônio que protege o planeta Terra dos raios solares.
Outro exemplo, a substância que mantém todos nós vivos, também é uma substância simples, O + O = O2 = gás oxigênio que respiramos que nos mantém vivos.
Mais um exemplo de substância simples, é o gás hidrogênio, um tipo de gás que pode ser usado como combustível para carros. H + H = H2 = gás hidrogênio.
X
-
1FSUBSTÂNCIA COMPOSTA
Texto em PortuguêsSUBSTÂNCIA COMPOSTA
Na natureza os átomos se combinam e formam as moléculas. Quando dois, três, ou mais átomos diferentes se combinam formam-se moléculas que representam substâncias compostas.
A substância água que você conhece e que é muito abundante no nosso planeta, essencial para a manutenção da vida na Terra, é formada por dois tipos de átomos diferente, o hidrogênio e o oxigênio. Para formar a água dois hidrogênio e um oxigênio se combinam.
H + O + H = H2O = água. Por isso a água é um exemplo de substância composta.
Um outro exemplo de substância composta é o gás carbônico ou dióxido de carbono (CO2). esse gás pode ser produzido e liberado no processo de respiração dos seres vivos, também na queima de combustíveis dos carros. O + C + O = CO2 = gás carbônico.
X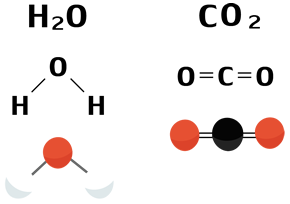
-
1GELEMENTO (Químico)
Texto em PortuguêsELEMENTO (Químico)
Na natureza encontramos vários tipos de átomos, aproximadamente 120 tipos de átomos. Átomo do mesmo tipo, são aqueles que possuem a mesma quantidade de prótons. Na química chamamos de elemento (químico) o conjunto de átomos que possuem o mesmo número de prótons, ou seja, conjunto de átomos do mesmo tipo, iguais. Os químicos representam os elementos por letras. Exemplo: C = cálcio; Ca = Carbono; N = nitrogênio; Na = sódio.
X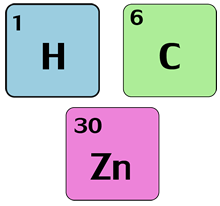
-
1HTABELA PERIÓDICA
Texto em PortuguêsTABELA PERIÓDICA
Para organizar os elementos, o químico russo Dimitri Mendeleev em 1869 organizou os elementos (químicos) em uma tabela.
A tabela periódica é uma ferramenta muito útil para os químicos e estudantes de química, pois a tabela periódica classifica e organiza os elementos (químicos) em função das suas propriedades e características.
Mendeleev não foi o primeiro a organizar os elementos em uma tabela, outros químicos já haviam feito isso antes dele, mas não deram muito certo… Na tabela periódica de Mendeleev, os 63 elementos conhecidos na época foram organizados em ordem crescente de massa atômica.Porém, a tabela periódica como conhecemos hoje foi criada pelo químico inglês Henry Moseley, em 1913. Moseley organizou os elementos em ordem crescente de número atômico (tabela periódica atual), que é o número de prótons que um átomo possui. Atualmente são conhecidos 118 elementos químicos. Dentre esses, 92 são naturais e 26 são artificiais.
X
-
1INÚCLEO
Texto em PortuguêsNÚCLEO
O átomo que é a menor parte da matéria (material) é formado por duas regiões: núcleo e eletrosfera.
Núcleo é a parte central do átomo, onde está concentrada a massa. No núcleo do átomo estão os prótons (partículas +) e os nêutrons (partículas sem carga).
O núcleo é a menor parte do átomo podendo ser de 10.000 a 100.000 vezes menor que o tamanho do átomo.
Podemos dizer então que o núcleo do átomo é:
Pesado, pois é nele que a massa está concentrada;
Pequeno, pois seu tamanho pode variar de 10.000 a 100.000 vezes menor que o tamanho do átomo;
Positivo, pois é no núcleo que estão os prótons (partículas positivas).
X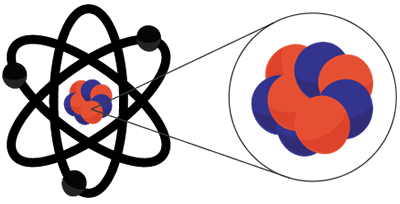
-
1JELETROSFERA
Texto em PortuguêsELETROSFERA
O átomo que é a menor parte da matéria (material) é formado por duas regiões: núcleo e eletrosfera.
Eletrosfera é a parte externa que envolve o núcleo. Na eletrosfera do átomo estão os elétrons (partículas -).
Ao contrário do núcleo, a eletrosfera do átomo é:
Leve, pois nela estão apenas os elétrons que possuem massa desprezível, insignificante;
Grande, pois seu tamanho pode variar de 10.000 a 100.000 vezes maior que o tamanho do núcleo;
Negativa, pois é na eletrosfera que estão os elétrons (partículas negativas).
X
-
1KMATÉRIA
Texto em PortuguêsMATÉRIA
Tente se imaginar em algum lugar familiar, como sua casa, sua escola, no ônibus, enfim, você consegue perceber quantos materiais diferentes compõem estes ambientes? Sabe o que todos esses materiais diferentes têm em comum? Todos são formados por átomos.
Átomo é a menor parte que constitui qualquer material. Toda material então, é formado por minúsculas partículas, os átomos. Ou seja, Tudo é formado por átomo. Exemplos: os alimentos, o ar, nossas roupas, o vidro do carro, o celular, a geladeira, tudo, tudo é formado por átomos, inclusive nós!
Todo átomo tem massa, então tudo tem massa, não importa se é gás, líquido ou sólido, tudo tem massa, porque tudo tem átomo.
Os químicos usam a palavra M-A-T-É-R-I-A, quando se referem aos materiais. Então toda matéria tem massa, como por exemplo uma formiguinha tem massa, um elefante tem massa. E a formiga, assim como o elefante também, ocupam lugar no espaço. Claro que um elefante ocupa mais espaço que uma formiguinha, né?
Podemos concluir que se tudo na natureza é formado por átomos, então tudo tem massa e tudo ocupa lugar no espaço (volume).
Então, M-A-T-É-R-I-A, (apresentar o sinal de matéria) é tudo que tem massa e ocupa lugar no espaço. Massa (m) e volume (V) são propriedades de toda matéria. Exemplos de matéria: plástico, metal, madeira, vidro e muitos mais.
X
-
1LCOMPOSIÇÃO
Texto em PortuguêsCOMPOSIÇÃO
Você já se perguntou como é possível existir tantos materiais diferentes? Tem diferentes tipos de plástico, diferentes tipos de metal, diferentes tipos de tecidos. Você sabe como isso é possível? A Química explica: Depende do que o material é feito! Ou seja, depende da composição do material. Composição significa do que é feito o material. Vinagre, conhece? A composição do vinagre é 4% de ácido acético (C2H4O2) e 96% de água (H2O), a composição de uma aliança de casamento é 75% de ouro (Au) e os outros 25% são de prata (Ag) e cobre (Cu).
X

-
1MPROPRIEDADE
Texto em PortuguêsPROPRIEDADE
É o que confere característica a um determinado material, exemplo: os metais conduzem eletricidade, os plásticos não conduzem, o álcool dissolve na água, o óleo não dissolve, o açúcar derrete à 160ºC, o sal de cozinha derrete à 801ºC.
X

-
1NRESUMO

Resumo da Unidade I
Estamos chegando ao fim da Unidade I, estudamos sobre conteúdos muito importantes sobre Química. Vimos que:
- A Química é uma Ciência que estuda a matéria, sua composição, propriedades e transformação.
- Toda matéria é formada por uma estrutura comum e muito pequena que são os átomos. Os átomos se tornam estáveis quando se combinam com outros átomos iguais ou diferentes.
- As moléculas são grupos de átomos que se combinam e são representadas por fórmulas, com H2O.
- Uma substância possui propriedades e característica próprias. Existem dois tipos de substâncias: substância simples, quando formada por átomos iguais, exemplo: O2; substância composta, quando formada por átomos diferentes, exemplo: CO2.
- Para cada tipo de átomo existente na natureza os químicos representam por um elemento, que é representado por uma letra e encontra-se na tabela periódica.
- O átomo tem duas regiões: Núcleo e eletrosfera. O núcleo é pequeno, pesado e positivo, dentro do núcleo tem próton (+) e nêutron. A eletrosfera é grande, leve e negativa, dentro da eletrosfera tem elétrons (-).
- Toda matéria tem massa e volume, pois é formada de átomos. A composição da matéria irá definir suas propriedades.
- Contato: glossario_quimica@ifsc.edu.br
2020 © Comunicação IFSC Palhoça Bilíngue | Projeto de Mestrado da professora Karina Zaia Machado Raizer